Abstrak
Limbah dan produk sampingan penangkapan ikan, baik yang terjadi secara alami maupun dari pemrosesan industri, merupakan sumber penting senyawa bernilai tinggi. Pupuk, biomaterial, kosmetik, biopelumas, dan biodiesel adalah beberapa zat yang dapat diperoleh dari residu ini. Tujuan dari penelitian ini adalah untuk melakukan penyelidikan teoritis dan eksperimental tentang produksi biokatalitik etil ester melalui hidroesterifikasi enzimatik dari minyak nila residu ( Oreochromis niloticus ). Lipase Eversa Transform 2.0 digunakan selama tahap esterifikasi, dengan metodologi Taguchi diterapkan untuk menilai efek dari berbagai parameter: suhu (25, 40, dan 55 °C), rasio molar asam lemak bebas (FFA) terhadap etanol (1:1, 1:5, dan 1:9), konsentrasi biokatalis (1%, 5%, dan 9%), dan waktu reaksi (1, 3, dan 5 jam). Analisis statistik mengungkapkan bahwa jumlah biokatalis merupakan faktor yang paling signifikan, diikuti oleh suhu. Kadar optimal yang diidentifikasi adalah 5 jam reaksi pada suhu 25 °C, dengan rasio molar 1:1 (FFA/etanol) dan 9% biokatalis, yang menghasilkan konversi eksperimental sebesar 89,94 ± 0,09%. Studi docking dan dinamika molekuler juga dilakukan, mengevaluasi stabilitas lipase Eversa Transform 2.0 dengan FFA, dan penggabungan situs katalitik enzim dengan substrat diamati. Asam miristat dan asam oleat terikat di dekat situs aktif enzim, menunjukkan energi bebas yang menguntungkan dan membentuk ikatan hidrogen, interaksi alkil, dan interaksi π -alkil, seperti yang diungkapkan oleh studi in silico . Penelitian ini selaras dengan Tujuan Pembangunan Berkelanjutan (SDGs) utama, termasuk SDG 7 (Energi Terjangkau dan Bersih) dan SDG 9 (Industri, Inovasi, dan Infrastruktur), dan SDG 12 (Konsumsi dan Produksi yang Bertanggung Jawab), dengan mendorong penggunaan energi terbarukan dan mendukung proses industri yang lebih berkelanjutan.
Perkenalan
Penggunaan minyak sayur berbiaya tinggi (minyak bunga matahari, minyak kedelai, minyak lobak, atau minyak kanola) untuk sintesis biodiesel secara ekonomi tidak kompetitif dibandingkan dengan minyak solar. 1 – 3 Penggunaan bahan baku yang dapat dimakan untuk sintesis biofuel juga dapat menimbulkan dampak buruk, terutama di negara-negara berkembang. 1 , 4 , 5 Minyak sayur yang tidak dapat dimakan (seperti minyak jarak, minyak biji kapas, minyak nimba, dan minyak biji pohon karet) telah dieksplorasi sebagai bahan baku alternatif, termasuk asam lemak yang berasal dari alga dan lemak hewani. 6 – 8 Lemak hewani berasal dari pengolahan daging, dan minyak ikan merupakan salah satu produk sampingan dari proses ini. 9 – 11
Produksi hewan akuatik global meningkat sebesar 4% dari tahun 2020 ke titik tertinggi baru sebesar 185 juta ton (setara berat hidup) pada tahun 2022, akuakultur menyumbang USD 296 miliar terhadap nilai penjualan perdana global yang diproyeksikan sebesar USD 452 miliar. 12 Di Brasil, ikan nila ( Oreochromis niloticus ) merupakan spesies yang dominan dalam akuakultur ikan. 13 , 14 Namun, lebih dari separuh berat tubuh ikan terbuang selama pemrosesan, dan minyak ikan residu, yang terdapat dalam jumlah bervariasi dalam daging, kepala, rangka, sirip, ekor, kulit, dan usus ikan, biasanya mengandung 2%–30% lemak. Ini merupakan potensi yang kuat untuk valorisasi – terutama untuk konsumsi manusia atau produksi biodiesel. 15 – 17 Minyak ikan residu menawarkan nilai kalor yang tinggi, biodegradabilitas, dan efisiensi pembakaran, yang menunjukkan potensinya sebagai alternatif bahan bakar berbasis minyak bumi. 18 Penelitian lebih lanjut tentang metode produksi sangat penting untuk mendukung penerapannya yang efektif. 19 – 21
Metode esterifikasi atau transesterifikasi biasanya digunakan dalam produksi biodiesel dan dapat dikatalisis menggunakan agen kimia atau enzimatik. 22 – 24 Metode utama yang digunakan untuk produksi biodiesel adalah transesterifikasi tetapi metode ini memiliki persyaratan khusus terkait kadar air bahan baku dan asam lemak. 25 Katalis biasanya berupa senyawa kimia dengan unsur-unsur yang sangat basa. 26 Namun, jalur kimia memiliki kekurangan, seperti menghasilkan limbah yang mencemari, konsumsi energi yang tinggi, dan kompleksitas proses pemulihan gliserol. 27 – 29
Hidroesterifikasi menghadirkan solusi yang layak untuk mengatasi tantangan dalam memproduksi biodiesel dari bahan baku dengan kadar asam lemak bebas (FFA) dan air yang tinggi. 30 – 32 Pendekatan ini umumnya digunakan untuk mengatasi tantangan dalam produksi tradisional substrat generasi kedua, seperti lemak hewani dan berbagai minyak yang tidak dapat dimakan. 33 Produksi biodiesel melalui hidroesterifikasi melibatkan proses dua tahap yang terdiri dari reaksi hidrolisis dan esterifikasi berturut-turut. 34 , 35 Pada tahap pertama, mono- dan triasilgliserol dihidrolisis untuk menghasilkan asam lemak dan gliserol; pada tahap kedua, asam lemak diesterifikasi untuk menghasilkan biodiesel. 36
Produksi biodiesel enzimatik telah mengalami kemajuan yang signifikan karena pengembangan biokatalis yang lebih efisien, seperti lipase yang diimobilisasi, yang meningkatkan stabilitas dan penggunaan ulang enzim. 37 – 39 Teknik-teknik baru, seperti pelarut eutektik dalam dan reaktor aliran kontinu, telah mengoptimalkan konversi minyak sayur dan limbah lemak menjadi biodiesel, sehingga mengurangi biaya dan dampak lingkungan. 40 – 42 Kemajuan dalam rekayasa genetika juga memungkinkan modifikasi mikroorganisme untuk menghasilkan lipase yang lebih spesifik dan tangguh, sehingga proses ini lebih layak dalam skala industri. 43 – 45 Kemajuan ini memperkuat potensi biodiesel enzimatik sebagai alternatif berkelanjutan untuk bahan bakar fosil. 46 – 48
Katalisis enzimatik memberikan manfaat yang signifikan pada teknik transesterifikasi tradisional yang dikatalisis oleh asam dan basa, khususnya saat mengubah minyak residu dengan konsentrasi FFA yang tinggi. 49 Meskipun transesterifikasi basa memiliki efisiensi konversi yang tinggi, sensitivitasnya terhadap FFA menyebabkan produksi sabun, sehingga memerlukan langkah pra-perlakuan. 50 Sebaliknya, transesterifikasi yang dikatalisis oleh asam tidak terlalu terpengaruh oleh FFA tetapi dibatasi oleh periode reaksi yang lebih panjang dan reagen yang lebih korosif. 51 Katalisis enzimatik menghilangkan kebutuhan untuk pra-perlakuan minyak dan berfungsi pada suhu dan tingkat pH yang lebih rendah, menghemat energi dan mengurangi pembentukan produk sampingan yang tidak diinginkan. 52
Enzim berfungsi sebagai katalis biologis yang memfasilitasi konversi spesies kimia dalam sistem kehidupan. 53 , 54 Enzim dapat mengkatalisis reaksi dalam kondisi ringan sambil menunjukkan spesifisitas substrat yang tinggi, sehingga meminimalkan produksi produk sampingan. 55 , 56 Enzim juga berasal dari sumber daya yang terbarukan, dapat terurai secara hayati, dan biokompatibel; penggunaannya mengurangi biaya pembuangan residu logam dari produk. 57 , 58 Menurut International Union of Biochemistry (IUB), enzim dapat diklasifikasikan ke dalam kategori berikut: oksidoreduktase, transferase, hidrolase, liase, isomerase, dan ligase.
Lipase, subkelas hidrolase, adalah enzim karboksil esterase yang berasal dari hewan, tumbuhan, atau mikroorganisme seperti bakteri, jamur, atau khamir. Mereka juga dikenal sebagai hidrolase triasilgliserol (EC 3.1.1.3). 59 , 60 Enzim-enzim ini dapat menghidrolisis asil gliserol rantai panjang, 61 dan relevansinya karena keserbagunaannya dalam mengkatalisis berbagai reaksi seperti transesterifikasi, 62 esterifikasi, 63 interesterifikasi, 64 hidrolisis, 65 alkoholisis, 66 asidolisis, 67 dan aminolisis. 68 Potensi bioteknologi lipase disebabkan oleh stabilitasnya yang tinggi dalam pelarut organik, kurangnya kofaktor, spesifisitas substrat yang luas, dan enantioselektivitas yang tinggi. 69
Candida antarctica, Thermomyces lanuginosus , dan Burkholderia cenocepacia merupakan lipase mikroba yang sering digunakan. Lipase dari Candida antarctica (A dan B) dikenal luas karena keserbagunaannya, menonjol dalam aplikasi seperti sintesis organik, produksi senyawa kiral, dan proses dalam industri makanan dan kosmetik. 70 , 71 Lipase Thermomyces lanuginosus (TLL) stabil pada suhu dan pelarut tinggi, sehingga cocok untuk berbagai aplikasi, termasuk degradasi residu lipid dan minyak serta modifikasi lipid untuk produk kosmetik. 72 Lipase Burkholderia cenocepacia (BCL) lebih menyukai trigliserida dan ester rantai panjang dan tahan terhadap pelarut organik. 73 , 74
Lipase Eversa Transform 2.0 (ET2) adalah enzim hasil rekayasa genetika yang secara industri berasal dari lipase T. lanuginosus (TLL), yang diproduksi melalui fermentasi terendam dari strain Aspergillus oryzae hasil rekayasa genetika . 75 Eversa Transform 2.0 dirancang terutama untuk memproduksi biodiesel menggunakan bahan baku dengan kandungan FFA, dari minyak dengan keasaman rendah hingga tinggi seperti minyak residu. Enzim ini memiliki 269 residu asam amino, berat molekul yang setara dengan 31,5 kDa, dan aktivitas 9100 IU·mL −1 . 76 Enzim dapat digunakan dalam berbagai industri (kosmetik, makanan, biofuel), dan penggunaannya dalam proses perlu dioptimalkan untuk memastikan kelayakan industrinya. 19 , 77 , 78
Dengan demikian, parameter seperti rasio molar, suhu, persentase biokatalis, dan waktu reaksi memengaruhi hasil dan efisiensi proses 26 , 79 Parameter ini penting, karena memilih kondisi yang tidak memadai dapat membahayakan stabilitas enzim, meningkatkan biaya atau mengurangi konversi asam lemak menjadi etil ester. 31 , 80 , 81 Alat statistik, seperti metode Taguchi, dapat membantu mengidentifikasi kombinasi parameter yang optimal pada tingkat yang ditentukan sambil meminimalkan jumlah eksperimen yang diperlukan dan menghemat sumber daya. 82 – 84 Selain meningkatkan efisiensi proses, metodologi ini menawarkan pendekatan sistematis untuk mengatasi kompleksitas biokatalisis, menjadikannya opsi yang hemat biaya dan kompetitif untuk produksi biodiesel industri. 85 – 87 Selain manfaat metode Taguchi, alat komputasi juga menyediakan kemampuan berharga untuk menganalisis dan meningkatkan setiap langkah proses produksi.
Penelitian molekular, docking, dan dinamika molekular merupakan beberapa metode komputasi relevan yang digunakan untuk menggambarkan interaksi antara enzim dan substrat guna menciptakan proses yang efektif dan optimal. 88 – 90 Dinamika molekular memungkinkan pengamatan ketahanan dan adaptasi interaksi ini dalam pengaturan simulasi, sedangkan analisis docking memberikan informasi tentang mekanisme pengikatan enzim dan afinitasnya terhadap substrat. 91 – 93 Informasi ini penting untuk menjelaskan variabel yang memengaruhi kinerja katalitik dan untuk memberikan bukti modifikasi eksperimental yang mengoptimalkan produksi biodiesel.
Tujuan dari artikel ini adalah untuk mengeksplorasi potensi inovatif minyak nila sisa ( Oreochromis niloticus ) untuk produksi biodiesel dengan hidroesterifikasi enzimatik. Ini menggunakan metode Taguchi untuk menganalisis hasil, mengoptimalkan proses sintesis, dan menyelidiki bagaimana berbagai parameter reaksi (rasio molar, biokatalis, suhu, dan waktu) dapat memengaruhi konversi. Akhirnya, ia menerapkan konsep kimia teoritis untuk mempelajari dinamika molekuler dan kopling selama reaksi enzimatik, menggunakan lipase Eversa Transform 2.0 sebagai biokatalis. Pendekatan ini memajukan pemahaman kita tentang produksi biodiesel dari bahan baku alternatif dan mengintegrasikan teknik optimasi dan analisis molekuler terkini, menandai langkah maju yang signifikan di bidang ini. Selain itu, penelitian ini berkontribusi pada beberapa Tujuan Pembangunan Berkelanjutan (SDGs), termasuk SDG 7 (Energi Terjangkau dan Bersih), SDG 9 (Industri, Inovasi, dan Infrastruktur), dan SDG 12 (Konsumsi dan Produksi yang Bertanggung Jawab), dengan mempromosikan sumber energi terbarukan dan mendorong praktik industri yang berkelanjutan.
Metodologi
Bahan
Penelitian ini menggunakan lipase komersial Eversa transform 2.0 dari A. oryzae dan lipase dari T. lanuginosus , yang keduanya diperoleh dari Sigma-Aldrich Brasil Ltda (Cotia, São Paulo, Brasil). Semua reagen kimia lain yang digunakan bermutu analitis dan disediakan oleh Synth (São Paulo, Brasil) dan Vetec (São Paulo, Brasil). Desain eksperimen penelitian ini dikembangkan menggunakan perangkat lunak Statistica 10 yang canggih, yang menggunakan metode Taguchi. Minyak nila residu yang digunakan dalam penelitian ini diperoleh melalui upaya kolaboratif dengan perusahaan budidaya ikan di Ceará, Brasil.
Metode
Studi eksperimental
Tahap hidrolisis: melakukan hidrolisis enzimatik untuk mengekstraksi asam lemak bebas (FFA)
Awalnya, minyak nila ( Oreochromis niloticus ) yang tersisa (nilai asam: 41,56 mg KOH/g) dihidrolisis dengan katalisis enzimatik menggunakan lipase T. lanuginosus . Artikel ini mengikuti metodologi yang diusulkan dalam literatur 94 dengan beberapa adaptasi. Larutan minyak:air dengan volume yang setara disiapkan. Campuran dipertahankan pada suhu 40 °C, dengan penambahan biokatalis 0,4% (relatif terhadap massa minyak), dan diaduk terus-menerus selama 4 jam pada suhu konstan. 94
Larutan tersebut kemudian dipindahkan ke corong pemisah untuk pemisahan fase. Air suling, yang sebelumnya dipanaskan hingga 60° C, ditambahkan, dan fase air dibuang. Asam lemak bebas dicuci tiga kali dan dipanaskan selama 10 menit pada suhu konstan 80° C. Natrium sulfat anhidrat digunakan selama penyaringan untuk menghilangkan kelembapan. Akhirnya, FFA disimpan dalam botol berwarna kuning.
Tahap esterifikasi: optimalisasi esterifikasi enzimatik yang ditujukan untuk produksi biodiesel, memanfaatkan metode Taguchi untuk analisis variabel
Empat parameter dikelompokkan ke dalam tiga tingkat menggunakan matriks ortogonal L9 konvensional berdasarkan metode Taguchi untuk meningkatkan efisiensi konversi ester. Sebutan ‘L’ dan ‘9’ masing-masing menunjukkan kotak Latin dan jumlah percobaan. Tabel 1 menggambarkan empat variabel independen (rasio molar, biokatalis, suhu, dan waktu) beserta nilai-nilai yang sesuai. Volume reaksi digunakan untuk menentukan persentase biokatalis setelah perhitungan rasio molar.
| Tingkatan | Rasio molar (v:v) | Biokatalis (%) | Suhu (°C) | Waktu (h) |
|---|---|---|---|---|
| Tingkat 1 (L1) | 1:1 | 1 | 25 | 1 |
| Tingkat 2 (L2) | 1 jam 5 menit | 5 | 40 | 3 |
| Tingkat 3 (L3) | skala 1:9 | 9 | 55 | 5 |
Karena penelitian ini bertujuan untuk meningkatkan respons (konversi asam lemak), nilai rasio sinyal terhadap derau (S/N) yang sesuai dengan pelapis ditentukan menggunakan karakteristik khusus fungsi ‘semakin besar semakin baik’. Metode Taguchi menggunakan rasio S/N untuk mengevaluasi karakteristik kualitas dan penyimpangan dari nilai yang diinginkan. Sistem bekerja dengan baik ketika rasio S/N digunakan untuk menilai data, karena sistem menjadi kurang sensitif terhadap penyebab fluktuasi. 96 Untuk setiap percobaan, rasio S/N dihitung menggunakan Persamaan ( 1 ):

Metode analitis
Nilai asam
Nilai asam awal dan akhir (setelah langkah hidrolisis) dihitung dari Persamaan ( 3 ). Aliquot sebanyak 0,2 g dikeluarkan dari volume campuran reaksi akhir dan diencerkan dalam 5 mL etil alkohol dan ditambahkan 3 tetes fenolftalein, kemudian dititrasi dengan larutan natrium hidroksida 0,1 mol·L −1 .

Resonansi magnetik nuklir proton
Spektrum satu dimensi resonansi magnetik nuklir hidrogen ( 1 H NMR) dan resonansi magnetik nuklir karbon ( 13 C NMR) diperoleh menggunakan spektrometer Bruker (Billerica, MA, AS), model Advance DRC-300, yang ditempatkan di Northeastern Center for the Application and Use of Magnetic Resonance di Federal University of Ceará (CENAUREMN-UFC). Frekuensi hidrogen adalah 500 MHz, dan frekuensi karbon adalah 75 MHz. Kloroform terdeuterasi (CDCL3) berfungsi sebagai pelarut untuk pelarutan sampel, dan sampel dianalisis dalam tabung 5 mm. 29
Kromatografi cair kinerja tinggi
Sebagian kecil dari media reaksi diekstraksi pada titik konversi optimum dan dianalisis menggunakan kromatografi cair kinerja tinggi (HPLC) dengan kolom LC-18 Shimadzu (Kyoto, Jepang) dan detektor ultraviolet. Metode isokratik digunakan dengan campuran 30% asetonitril dan 70% metanol. Volume 20 μL disuntikkan per menit selama 5 menit pada suhu 40 °C, dengan panjang gelombang 254 nm dipilih karena penyerapannya yang lebih tinggi dalam spektrum. 29
Kepadatan pada suhu 20 °C dan viskositas kinematik pada suhu 40 °C
Kepadatan pada suhu 20 °C ditentukan menurut prosedur yang diuraikan dalam standar ASTM D-7042. Viskometer digital Anton Paar SVM 3000-Stabinger (Gaz, Austria) digunakan untuk pengukuran. Viskositas kinematik pada suhu 40 °C ditentukan mengikuti metodologi yang diuraikan dalam standar ASTM D-70422. Viskometer digital Anton Paar SVM 3000-Stabinger juga digunakan untuk tujuan ini.
Studi teoritis
Persiapan pengikat dan protein
Struktur molekul komponen lipid minyak ikan menggunakan Eversa 2.0 dihasilkan dengan perangkat lunak Chem3D 97 (Gbr. 1 ). Untuk optimasi otomatis, medan gaya MMFF94S 98 diterapkan untuk menghasilkan konformasi bioaktif dengan meminimalkan konformer yang dihasilkan secara acak menggunakan algoritma Steepest Descent, 99 dengan empat langkah per pembaruan, 100 dalam perangkat lunak AVOGADRO. 101 File ligan kemudian dikonversi ke format .pdbqt menggunakan OpenBabel v. 3.0.0, 102 dengan status ionisasi dan tautomerik yang disesuaikan dengan pH 7,4. 102
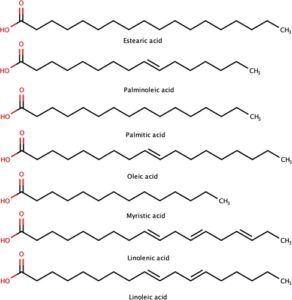
Reseptor yang diteliti adalah lipase Eversa 2.0, yang dimodelkan menurut prosedur yang ditetapkan, 103 , 104 berdasarkan struktur kristal yang diperoleh melalui difraksi sinar-X. Residu yang mengganggu, molekul air, dan inhibitor sintetis dihilangkan untuk memungkinkan docking molekuler. Hidrogen polar ditambahkan secara terpisah ke ligan dan protein. Teknik ini memungkinkan penyaringan basis data ligan virtual terhadap target protein tertentu. Perangkat lunak yang digunakan adalah AutoDock Tools. 105
Docking molekuler
Docking molekular dilakukan menggunakan AutoDock Vina, 106 yang menggunakan three-way multithreading dan Algoritma Genetika Lamarckian. Untuk docking kompleks protease utama Eversa 2.0, parameter berikut digunakan: ukuran grid (30 × 30 × 30), jarak (0,642), dan koordinat pusat grid (−34.282188, 24.937188, 73.691625). Semua parameter lainnya ditetapkan sebagai default. Ligand input, dalam format .pdbqt dengan hidrogen polar, digunakan. Antara 10 dan 40 kali docking dilakukan, dan frekuensi pose docking yang diulang di wilayah reseptor yang sama direkam. Untuk memvalidasi kinerja simulasi dan menilai kualitas docking, kriteria penilaian deviasi kuadrat rata-rata (RMSD) diterapkan, dengan docking yang berhasil didefinisikan sebagai RMSD 2,0 Å atau lebih rendah. 107 Interaksi reseptor-ligan utama divisualisasikan menggunakan Discovery Studio 108 dan PyMOL. 109
Analisis statistik
Hasil dinyatakan sebagai nilai rata-rata ± standar error dari rata-rata. Setelah mengonfirmasi distribusi normal dan homogenitas data, perbedaan antar kelompok dilakukan analisis varians (ANOVA satu arah) dan ANOVA dua arah dalam percobaan dengan antagonis, diikuti oleh uji Tukey. Semua analisis dilakukan menggunakan perangkat lunak GraphPad Prism v.8.0. Tingkat signifikansi statistik ditetapkan pada 5% ( P < 0,05).
Dinamika molekul
Simulasi dinamika molekul (MD) dilakukan menggunakan program NAMD. 112 Konformasi terbaik dari docking molekul dilarutkan dalam air TIP3P, 113 menggunakan medan gaya CHARMM36, dengan ion yang ditambahkan untuk menetralkan muatan bersih sistem. Minimalisasi energi kemudian dilakukan menggunakan metode Steepest Descent. Sistem selanjutnya diseimbangkan dalam ensembel NVT (jumlah partikel, volume, dan suhu konstan) dan NPT (jumlah partikel, tekanan, dan suhu konstan), sebagaimana didefinisikan oleh dinamika Langevin. 114 Simulasi produksi sistem dilakukan dengan waktu 100 ns. Kualitas struktur yang diperoleh dalam MD dievaluasi menggunakan parameter berikut dengan NAMD:
- Energi potensial (kkal·mol −1 ). 115
- Energi interaksi protein-ligan (kkal·mol −1 ).
- Deviasi kuadrat rata-rata posisi atomik protein, pengikat, dan jarak di antara keduanya (RMSD, Å), dan deviasi kuadrat rata-rata posisi inti protein, ligan, dan jarak di antara keduanya (RMSD, Å).
- Ikatan hidrogen dievaluasi menggunakan perangkat lunak Visual Molecular Dynamics (VMD). 116
- Fluktuasi kuadrat rata-rata jarak minimum antara protein dan ligan diamati dalam MD (RMSF, Å). 117 Grafik dibuat menggunakan program Qtrace. 118
Hasil dan Pembahasan
Studi eksperimental
Tahap hidrolisis: melakukan hidrolisis enzimatik untuk ekstraksi FFA
Indeks keasaman minyak sisa ikan nila meningkat dari 41,56 menjadi 94,64 mg KOH g −1 setelah hidrolisis enzimatik, yang menunjukkan keberhasilan pelepasan dan peningkatan FFA. Santos dkk . menggunakan minyak ikan nila untuk memperoleh asam lemak bebas untuk produksi biodiesel, menggunakan hidrolisis kimia (saponifikasi alkohol dengan natrium hidroksida diikuti oleh hidrolisis asam sulfat) yang dibantu oleh ultrasonik. 119 Dalam studi terpisah, hidrolisis minyak goreng sisa menggunakan campuran enzim juga menghasilkan hasil yang memuaskan. 120
Oleh karena itu, hidrolisis minyak residu sangat penting untuk menghasilkan produk bernilai tinggi, meskipun setiap metode memiliki tantangan tersendiri. Rute kimia melibatkan langkah pemisahan dan pemurnian tambahan, yang meningkatkan waktu dan biaya energi. Sebaliknya, rute enzimatik menawarkan spesifisitas yang lebih tinggi, meminimalkan produk sampingan yang tidak diinginkan, dan menghilangkan kebutuhan untuk pemurnian lebih lanjut.
Tahap esterifikasi: optimalisasi esterifikasi enzimatik yang ditujukan untuk produksi biodiesel, memanfaatkan metode Taguchi untuk analisis variabel
Metode Taguchi memungkinkan pengoptimalan parameter reaksi, sehingga secara signifikan mengurangi jumlah langkah eksperimen dalam proses tersebut. Dengan cara ini, dimungkinkan untuk mengidentifikasi kadar terbaik untuk setiap parameter, mengeksplorasi variasinya dalam desain eksperimen untuk mencapai konversi maksimum menjadi ester. Tabel 2 menyajikan nilai konversi yang diperoleh dan desain eksperimen lengkap, termasuk parameter, kadar, nilai yang sesuai, dan S/N untuk setiap eksperimen yang dianalisis. Reaksi diduplikasi, memastikan bahwa margin kesalahan tetap berada dalam standar yang diinginkan.
| Reaksi | Rasio molar | Biokatalis (% b/b) | Suhu (°C) | Waktu (h) | Konversi (%) | Nomor telepon |
|---|---|---|---|---|---|---|
| 1 | 1:1 | 1 | 25 | 1 | 61,5 ± 0,05 | 35.77 |
| 2 | 1:1 | 5 | 40 | 3 | 49,6 ± 0,17 | 33.90 |
| 3 | 1:1 | 9 | 55 | 5 | 70,1 ± 0,02 | 36.90 |
| 4 | 1 jam 5 menit | 1 | 40 | 5 | 48,8 ± 0,74 | 33.76 |
| 5 | 1 jam 5 menit | 5 | 55 | 1 | 50,1 ± 0,72 | 34.00 |
| 6 | 1 jam 5 menit | 9 | 25 | 3 | 83,8 ± 0,29 | jam 38.45 |
| 7 | skala 1:9 | 1 | 55 | 3 | 19,3 ± 0,38 | 25.72 |
| 8 | skala 1:9 | 5 | 25 | 5 | 74,4 ± 0,54 | 37.42 |
| 9 | skala 1:9 | 9 | 40 | 1 | 75,1 ± 0,41 | 37.50 |
Parameter yang paling memengaruhi reaksi adalah persentase biokatalis, diikuti oleh suhu. Hal ini mencerminkan saling ketergantungan mereka, karena enzim dapat mengalami denaturasi pada suhu tinggi, sehingga mengurangi aktivitas katalitik. 121 Aktivitas enzimatik menunjukkan kemampuan enzim untuk mengkatalisis reaksi tertentu, dan peningkatan konsentrasi enzim umumnya meningkatkan laju reaksi jika substrat mencukupi. 122 , 123 Persentase biokatalis sangat signifikan, dengan kadar yang lebih tinggi menghasilkan konversi yang lebih besar secara proporsional. Reaksi 6, 8, dan 9, yang memiliki persentase biokatalis tertinggi, berhubungan dengan dua dari tiga konversi tertinggi (Tabel 2 ).
Suhu juga menonjol di antara parameter lainnya. Enzim memiliki kisaran suhu optimal di mana aktivitasnya paling tinggi, dan pada suhu yang terlalu tinggi atau terlalu rendah, aktivitas enzim dapat menurun atau enzim dapat mengalami denaturasi, kehilangan bentuk fungsionalnya. 124 , 125 Oleh karena itu, karakteristik spesifik aktivitas katalitik lipase yang digunakan pada kisaran suhu yang dipelajari relevan. Lipase Eversa Transform 2.0 telah mengurangi aktivitas katalitik dalam reaksi yang dilakukan pada suhu di atas 45 °C tetapi dalam percobaan yang dilakukan pada suhu 40 °C, kinerjanya sebagai biokatalis ditingkatkan. 75 Reaksi 6, 8 dan 9 menunjukkan tingkat konversi tertinggi dalam desain eksperimen. Hasil ini dikaitkan dengan kombinasi konsentrasi biokatalis yang tinggi dan kisaran suhu di mana biokatalis mempertahankan aktivitasnya, tanpa gangguan signifikan dari efek termal (Tabel 2 ).
Di antara parameter dengan pengaruh paling kecil pada konversi etil ester adalah waktu reaksi dan rasio molar. Keduanya tidak dapat diabaikan tetapi dampaknya kurang signifikan dibandingkan faktor lainnya. Alkohol berlebih dapat menyebabkan denaturasi atau inaktivasi enzim, sehingga mengurangi hasil. Reaksi 7, yang menggunakan alkohol berlebih dan konsentrasi biokatalis terendah, menghasilkan konversi terendah dalam matriks eksperimen (19,3 ± 0,38%). Jumlah enzim yang digunakan secara langsung memengaruhi keseluruhan biaya proses.
Analisis sinyal terhadap derau (S/N)
Metodologi Taguchi memungkinkan evaluasi signifikansi parameter yang diteliti dengan memberikan nilai rasio signal-to-noise (S/N). Dalam studi ini, kriteria ‘semakin tinggi semakin baik’ diterapkan, karena nilai konversi yang lebih tinggi berhubungan dengan rasio S/N yang lebih baik. Tabel 3 menyajikan nilai S/N rata-rata untuk setiap level parameter dan variasinya masing-masing (delta), dihitung sebagai perbedaan antara nilai S/N tertinggi dan terendah. Nilai delta ini memungkinkan klasifikasi parameter berdasarkan pengaruhnya.
| Faktor/tingkatan | Rasio molar | Biokatalis | Suhu | Waktu |
|---|---|---|---|---|
| 1 | 35.53 | 31.76 | 37.22 | 35.76 |
| 2 | 35.41 | 35.11 | Tanggal 35.06 | 32.70 |
| 3 | 33.55 | 37.62 | 32.21 | Tanggal 36.03 |
| Delta | 1.98 | 5.86 | 5.01 | 3.33 |
| Peringkat | 4 | 1 | 2 | 3 |
Di antara parameter yang dianalisis, konsentrasi biokatalis dan suhu adalah yang paling berpengaruh, dengan nilai delta masing-masing 5,86 dan 5,01 (Tabel 3 ). Hal ini sejalan dengan hasil eksperimen, yang mengonfirmasi pentingnya variabel-variabel ini dalam proses. Peningkatan linear yang jelas dalam konversi diamati dengan meningkatnya kadar biokatalis, dengan rentang dari 1% (Level 1) hingga 9% (Level 3) terbukti sangat relevan. Sebaliknya, peningkatan suhu dari 25 °C (Level 1) hingga 55 °C (Level 3) menyebabkan penurunan yang nyata dalam nilai S/N rata-rata, kemungkinan karena denaturasi termal dari biokatalis berbasis protein, yang mengganggu aktivitas katalitiknya.
Mengingat temuan ini, penting untuk mempertimbangkan interaksi antara parameter yang paling berpengaruh dan parameter dengan signifikansi statistik yang lebih rendah. Relevansi konsentrasi biokatalis menjadi sangat jelas ketika dievaluasi bersamaan dengan variasi rasio molar. Ketika rasio molar meningkat dari 1:1 (Level 1) menjadi 1:9 (Level 3), penurunan kinerja diamati, yang menunjukkan bahwa alkohol berlebih dapat menyebabkan denaturasi triad katalitik enzim. Dengan demikian, Level 1 (1:1) muncul sebagai kondisi yang paling sesuai berdasarkan hasil S/N rata-rata.
Analisis varians
Analisis varians (ANOVA) dilakukan. Tabel 4 menyajikan nilai yang diperoleh, dengan nilai P yang menunjukkan signifikansi parameter yang diteliti.
| Faktor | Bahasa Inggris | DF | F | P | Kontribusi (%) |
|---|---|---|---|---|---|
| Rasio molar | (25.55) | (2) | – | – | – |
| Biokatalis | 1640.37 | 2 | 19.56 | 0,011 | 60.39 |
| Suhu | 1068.58 | 2 | 12.74 | 0,023 | 39.34 |
| Waktu | 7.34 | 2 | 0,09 | 0.782 | 0.27 |
| Total | 2716.29 | 6 | – | – | 100 |
Biokatalis dan suhu signifikan pada tingkat keyakinan 95%, dengan nilai P masing-masing sebesar 0,011 dan 0,023. Kontribusi biokatalis melebihi suhu, yaitu sebesar 53,31% berbanding 34,72% (Tabel 5 ). Berdasarkan analisis statistik, kondisi optimal untuk memaksimalkan konversi ester diidentifikasi sebagai 5 jam (Level 3), 25 °C (Level 1), rasio molar 1:1 (Level 1), dan konsentrasi biokatalis 9% (Level 3).
| Senyawa | ID PubChem | Energi (kkal·mol −1 ) | Nilai tukar RMSD (Å) |
|---|---|---|---|
| Asam linoleat | Nomor ID5280450 | -6,1 | 1.79 |
| Asam linolenat | ID5280934 | -5,9 | 1.74 |
| Asam palmitoleat | Nomor ID445638 | -5,8 | 1.66 |
| Asam palmitat | CID985 | -5,6 | 1.80 |
| Asam oleat | Nomor ID445639 | -5,6 | 2.00 |
| Asam stearat | ID5281 | -5,4 | 1.51 |
| Asam miristat | Kode CID11005 | -5.1 tahun 2015 | 1.38 |
Secara teoritis, kondisi optimum akan menghasilkan konversi yang setara dengan 96,73%, tetapi setelah menerapkan kondisi ini secara eksperimental, konversinya adalah 89,94 ± 0,09%. Metodologi ini memenuhi tujuan optimasi dengan memuaskan karena konversi yang lebih tinggi diperoleh dengan menggunakan suhu yang lebih rendah dan rasio molar 1:1 pada Level 1. Namun, konversi eksperimental lebih rendah daripada konversi teoritis.
Studi teoritis
Docking molekuler
Berdasarkan literatur, 126 dan dengan beberapa adaptasi, 127 studi simulasi penggabungan molekul ini digunakan untuk menjelaskan reaksi hidrolisis antara komposisi minyak ikan dan lipase Eversa. Molekul docking AutoDock Vina memungkinkan untuk mencantumkan energi afinitas dan RMSD ligan, seperti yang ditunjukkan pada Tabel 5 .
Semuanya terletak di wilayah yang sama dari situs aktif protein, yang biasanya dibentuk oleh triad katalitik (Ser-His-Asp), dalam kasus Eversa 2.0 Ser 153, His 268, dan Asp 206. 103 , 104
Konformasi near-attack (NAC) menunjukkan kompatibilitas konformasi yang mendorong interaksi efektif antara situs katalitik dan karbon elektrofilik dari gugus asil, sehingga meningkatkan efisiensi katalitik. 128 Dalam NAC yang umum, jarak antara oksigen Ser105 (CALB) atau Ser153 (Eversa) dan karbon karbonil adalah sekitar 3 Å. Atom-atom ini biasanya membentuk sudut sekitar 60°, tidak melebihi 90°, dengan oksigen karbonil. 129
Secara umum, ligan-ligan tersebut dekat dengan situs katalitik. Akan tetapi, di antara ligan-ligan yang dievaluasi, asam miristat (C) menunjukkan potensi reaksi, membentuk NAC dengan residu Ser 153, meskipun energi afinitasnya lebih rendah daripada yang lain. Di sisi lain, asam stearat (G) terbukti membentuk interaksi hidrofobik langsung dengan salah satu residu triad katalitik, His 268. Akan tetapi, hasil-hasil tersebut menunjukkan bahwa kombinasi substrat asam linoleat (A) dan lipase terbukti stabil, mungkin karena interaksi hidrofobik dan hidrofilik dalam esterifikasi studi penjangkaran. 130 Hubungan langsung antara peningkatan afinitas pengikatan dan peningkatan panjang rantai karbon ester-ester tersebut juga dapat diamati. Perpanjangan ini mungkin terkait dengan peningkatan interaksi antara ligan-ligan dan situs katalitik enzim. 131 Jenis residu yang terlibat dalam interaksi antara asam lemak bebas dan Eversa Transform 2.0 ditunjukkan pada Tabel 6 dan Gambar 2 .
| Substrat | Limbah yang terlibat | |
|---|---|---|
| Ikatan hidrogen | Interaksi hidrofobik | |
| Asam linoleat | Asp276 (2,08 kaki) | Phe 265, pro 207, Val 208, Val 98, leu 262, Ile 94, Arg 95 |
| Asam linolenat | Tyr 29 (3,30 kaki, 2,9 kaki) | Tyr 92, leu 283, Phe 265, Arg 286 |
| Asam palmitoleat | – | Leu 283, leu 285, Phe 265, Ile 94, Tyr 92 |
| Asam palmitat | Tyr 29 (3,00 kaki) | Tyr 92, Phe 265, Val 269, leu 282, leu 263, leu 262 |
| Asam oleat | Tyr 29 (3,01 Å) | Tyr 92, Ile 94, Phe 265, leu 282, Val 269 |
| Asam stearat | Trp 270 (3,15 Å) | Nya 268, Ile 94, Tyr 92, Phe 265, leu 283, Val 269 |
| Asam miristat | Ser 153 (2,95 kaki)
Tyr 29 (2,94 Å) |
Tyr 92, Phe 265, leu 283, Val 269, leu 285, Trp 270 |
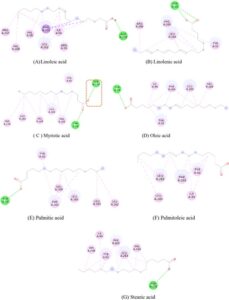
Dinamika molekul
Simulasi dinamika molekul
Deviasi akar kuadrat rata-rata (RMSD)
Ditemukan bahwa ligan yang diteliti ditampung dengan benar di situs katalitik lipase Eversa.132 Oleh karena itu, penelitian simulasi dilakukan pada kompleks lipase–ligan (Gbr. 3 ) untuk mengevaluasi tidak hanya perubahan konformasi enzim tetapi juga stabilitasnya setelah setiap perubahan konformasi. RSMD kompleks lipase-ligan digunakan untuk mengevaluasi sejauh mana perubahan konformasi terjadi pada molekul yang diteliti selama simulasi. Gambar 6 menunjukkan perilaku RSMD kompleks yang diteliti selama fase ekuilibrasi.
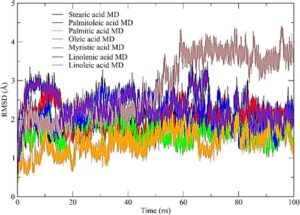
Dari simulasi kesetimbangan kompleks lipase–ligan dalam pelarut, dimungkinkan untuk memperoleh informasi awal tentang perilaku konformasi untuk dinamika. Pada langkah ini, nilai stabilisasi RSMD dari ligan yang dipelajari berfluktuasi antara 1,1 dan 4,2 Å selama periode yang dievaluasi. Nilai RSMD yang rendah ini mungkin terkait dengan pergerakan ion dan pelarut dalam sistem selama konformasi awal kompleks. Gambar 6 menunjukkan hasil yang diperoleh dalam fase produksi.
Seperti yang ditunjukkan pada Gambar 3 , asam miristat dan asam palmitat memiliki nilai RMSD rata-rata di bawah 2,0 Å. Di sisi lain, asam linolenat memiliki nilai sekitar 4,0 Å. Dengan demikian, hasil teoritis dan eksperimental yang disajikan dalam karya ini menunjukkan bahwa asam lemak dari minyak residu membentuk kompleks stabil dengan situs katalitik kompleks Eversa, yang dapat menunjukkan alternatif yang layak untuk aplikasi di masa mendatang.
Data yang disajikan dalam karya ini sesuai dengan hasil yang diperoleh dalam literatur, di mana penelitian telah mengevaluasi afinitas dan stabilitas molekuler berbagai asam lemak dengan lipase dalam reaksi esterifikasi. 131 Seperti dalam karya saat ini, penulis mengamati bahwa di antara kompleks yang dipelajari, asam oktadekanoat menunjukkan salah satu nilai RSMD tertinggi dan, oleh karena itu, salah satu nilai stabilitas terendah dibandingkan dengan kompleks lainnya.
Ikatan hidrogen
Ikatan hidrogen antarmolekul, landasan stabilitas kompleks enzim-ligan, telah lama menjadi fokus penelitian biokimia. Akan tetapi, sebuah penelitian terkini oleh Ragunathan et al . 133 menyelidiki ikatan ini secara lebih mendalam, khususnya dalam kompleks lipase-ligan, yang mengungkap wawasan baru menggunakan simulasi dinamika molekuler.
Dalam penelitian ini, analisis difokuskan terutama pada pemeriksaan pembentukan ikatan hidrogen antarmolekul antara ligan dan lipase selama fase keseimbangan dan produksi. Gambar 4 menunjukkan fluktuasi dalam jaringan ikatan hidrogen selama tahap-tahap ini, yang menjelaskan variasi dalam pembentukan ikatan. Penemuan penting adalah pembentukan ikatan hidrogen yang dinamis, dengan jumlah ikatan yang berfluktuasi antara satu dan tiga selama periode simulasi. Pengamatan asam miristat dan asam oleat menarik, yang menunjukkan pembentukan hingga tiga ikatan hidrogen selama lintasan 100 ns.

Terganggunya ikatan hidrogen mengindikasikan pergeseran stabilitas, yang sering dikaitkan dengan interaksi seperti gaya van der Waals atau gaya hidrofobik, seperti yang disoroti oleh Qin et al . 131 Analisis tersebut juga mengungkap korelasi langsung antara panjang rantai karbon ligan dan jumlah rata-rata ikatan, yang mengonfirmasi temuan dari studi docking molekuler sebelumnya. 134 Sebuah pengungkapan utama dari investigasi ini adalah perbedaan antara proses dinamis (dinamika molekuler) dan statis (docking molekuler), seperti yang dijelaskan oleh Fatma et al . 135 Meskipun docking molekuler memberikan wawasan berharga ke dalam interaksi statis, simulasi dinamika molekuler menangkap evolusi dinamis kompleks ini dan memberikan pemahaman yang lebih komprehensif tentang stabilitasnya.
Singkatnya, penyelidikan kami terhadap interaksi dinamis ikatan hidrogen antarmolekul dalam kompleks lipase–ligan memperdalam pemahaman kita tentang proses pengenalan protein-ligan dan memiliki implikasi signifikan bagi desain obat dan rekayasa enzim. Temuan ini menggarisbawahi relevansi praktis dan dampak penelitian kami.
Fluktuasi akar kuadrat rata-rata
Kami melakukan analisis RMSF terhadap sistem untuk menyelidiki dinamika dan stabilitas setiap residu protein sepanjang lintasan simulasi 100 ns. Gambar 5 menunjukkan interaksi utama dalam kompleks utama yang diselidiki, khususnya yang terdiri dari minyak ikan. Temuan tersebut mengisyaratkan adanya pergeseran konformasional yang substansial dalam kompleks lipase senyawa-Eversa selama periode simulasi.
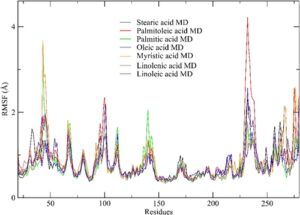
Hasil kami mengungkap fluktuasi yang konsisten dalam lintasan simulasi dinamika molekuler di seluruh kompleks, yang menunjukkan korelasi penting dengan residu replikasi utama, seperti yang disorot dalam literatur. 131 , 136 Hanya kompleks yang terbentuk antara metil dekanoat dan Eversa yang menunjukkan nilai RMSF yang melampaui 2,0 Å untuk residu Gly 47, Asp 100, Asn 232, dan His 268. Asam palmitoleat juga menunjukkan nilai RMSF di atas 4,2 Å, dalam residu Asn 232.
Meskipun terjadi fluktuasi yang diamati, hasil kami menunjukkan stabilitas struktur yang memuaskan dalam larutan berair. Konformasi yang diperoleh dari simulasi MD, yang dikomplekskan dengan berbagai ligan melalui teknik docking, memberikan wawasan penting tentang mode pengikatan molekul kecil di berbagai keadaan pelipatan enzim, seperti yang ditunjukkan dalam literatur. 137
Perhitungan luas permukaan yang dapat diakses pelarut
Studi ini memadukan simulasi dinamika molekuler (MD) dengan analisis Solvent Accessible Surface Area (SASA) untuk memberikan wawasan tentang perilaku protein dalam larutan. Simulasi MD 100 nanodetik dilakukan untuk memantau variasi SASA dalam kompleks protein yang terbentuk dengan komponen minyak ikan yang representatif. Hasilnya mengungkap perubahan konformasi yang bergantung pada waktu dan menawarkan informasi berharga tentang interaksi dinamis dan stabilitas struktural kompleks biomolekuler ini. 138
Analisis SASA kami menghasilkan tren yang menarik. Nilai SASA untuk senyawa tertentu, termasuk asam Palmitoleat, menunjukkan peningkatan yang nyata selama simulasi, yang menunjukkan relaksasi struktural. Sebaliknya, senyawa lain menunjukkan penurunan nilai SASA, yang menunjukkan ketegangan saat pembentukan kompleks dengan enzim (Gbr. 6 ). 139 , 140
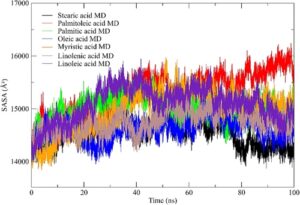
Dampak yang dapat diabaikan dari pengikatan ligan pada nilai SASA sangat menarik, menyiratkan bahwa interaksi ligan-protein tidak secara signifikan mengubah aksesibilitas pelarut ke permukaan protein. 143 Setelah 100 ns simulasi, nilai SASA stabil di sekitar konstanta, yang menunjukkan bahwa sistem yang diseimbangkan diambil sampelnya. Namun, yang menarik, kompleks dengan ion monovalen yang menstabilkan menunjukkan nilai SASA tertinggi – konsentrasi yang lebih tinggi berkorelasi dengan area yang lebih kecil, yang berpotensi menunjukkan pemadatan struktur protein yang disebabkan oleh muatan permukaan.
Sebagai kesimpulan, analisis SASA kami selama simulasi MD memberikan wawasan penting mengenai dinamika dan stabilitas kompleks komposisi minyak ikan. Temuan ini memperdalam pemahaman kita tentang perilaku protein dan dapat menginformasikan desain senyawa dengan interaksi protein-permukaan yang lebih baik atau kondisi yang dioptimalkan untuk pembentukan kompleks, yang menawarkan arah baru untuk penelitian dan aplikasi di masa mendatang.
Metode analitis
Kepadatan pada suhu 20 °C dan viskositas kinematik pada suhu 40 °C
Kepadatan dan viskositas kinematik merupakan indikator kinerja dan kompatibilitas utama untuk biofuel, yang juga memengaruhi biaya penyimpanan dan penanganan. Properti ini dinilai untuk membandingkannya dengan nilai standar yang ditetapkan oleh badan pengendalian mutu dan distributor nasional. Perhatian khusus diberikan pada viskositas kinematik pada suhu 40 °C dan kepadatan pada suhu 20 °C.
Berdasarkan Tabel 7 , nilai viskositas kinematik pada suhu 40 °C dan densitas pada suhu 20 °C untuk minyak yang diperoleh dalam penelitian ini berada dalam batas yang ditetapkan oleh ASTM International. Dibandingkan dengan nilai yang ditetapkan oleh Badan Perminyakan Nasional Brasil (ANP), hanya densitas yang berada dalam standar yang dipersyaratkan, sedangkan viskositas kinematik berada di bawahnya.
| Properti (Unit) | ASTM D6751 | Undang-Undang Nomor 920 Tahun 2023 | Pengarang | Referensi [ 141 ] | Referensi [ 142 ] |
|---|---|---|---|---|---|
| Viskositas kinematik pada suhu 40 °C, cSt | 1.9–6.0 | 3.0–5.0 | 2.47 | 5.14 | 5.34 |
| Kepadatan pada suhu 20 °C, kg·m − 3 | 860–900 | 850–900 | 883.6 | 798.7 | 877 |
Catatan : “cSt” mengacu pada centistokes, satuan viskositas kinematik.
Martins et al . memproduksi biodiesel dari minyak ikan menggunakan jalur kimia dengan katalis homogen, sehingga menghasilkan karakterisasi produk yang memuaskan. 142 Bioproduk mereka memenuhi standar ASTM D6751, tetapi menurut ANP 920/2023, hanya kepadatannya yang memenuhi standar. Dalam penelitian ini, minyak tersebut menunjukkan kepadatan yang lebih tinggi daripada yang dilaporkan oleh Martins et al ., sementara viskositas kinematiknya pada suhu 40 °C hanya setengahnya.
Smaisim et al . memilih rute biologis menggunakan enzim yang diimobilisasi untuk sintesis biodiesel dan menyajikan hasil yang memuaskan terkait sifat fisikokimia yang dievaluasi. 141 Minyak yang diproduksi oleh penulis menyajikan nilai yang lebih rendah dari batas yang ditetapkan oleh standar ASTM D6751 dan resolusi ANP 920/2023. Viskositas kinematik tetap dalam batas yang ditetapkan oleh standar internasional ASTM D6751, tetapi jika dibandingkan dengan standar nasional ANP 920/2023, viskositas kinematik tetap berada di luar batas yang ditunjukkan. Mengenai penelitian saat ini, diamati bahwa viskositas kinematik yang diperoleh oleh penulis lebih tinggi. Namun, densitasnya lebih rendah.
Resonansi magnetik nuklir
Dalam spektrum 1 H NMR (500 MHz, CDCl 3 ) dari media reaksi, dimungkinkan untuk mengamati sinyal untuk ester yang terbentuk. Meskipun spektrum campuran reaksi menunjukkan beberapa puncak yang tumpang tindih, dimungkinkan untuk menyorot puncak yang paling penting sebagai kriteria untuk menentukan keberadaan produk-produk ini dalam media reaksi. Gambar 7 menyorot beberapa pergeseran kimia yang signifikan dari etil oleat. Penjelasan untuk atom-atom hidrogen yang disorot dalam struktur etil oleat telah ditambahkan ke Gambar 7 untuk mengidentifikasi dan menetapkan sinyal-sinyal ke nilai pergeseran kimia dan multiplisitas sinyal masing-masing.
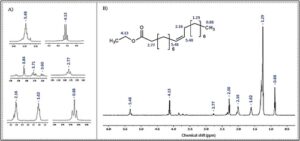
Sinyal dengan pergeseran kimia mendekati δ 5,48 dikaitkan dengan atom hidrogen dari karbon sp2. Karena pola pemisahannya yang khas untuk alkena, profil kimia ini menghasilkan sinyal multiplet. Sinyal pada δ 4,13 adalah kuartet, yang sesuai dengan keragaman dan pergeseran kimia yang dikaitkan dengan hidrogen yang terikat langsung pada oksigen dari gugus ester. Puncak pada δ 3,84, δ 3,71, dan δ 3,60 dikaitkan dengan ester yang lebih encer dalam media reaksi karena intensitasnya yang rendah dalam spektrum. Triplet yang diamati pada δ 2,77 merupakan karakteristik hidrogen metilen dalam posisi α pada karbonil ester. Sinyal yang diamati pada δ 1,29 dan δ 1,62 terkait dengan gugus metil dan metilen yang umum pada ester dalam media reaksi. Akhirnya, sinyal pada δ 0,88 dikaitkan dengan gugus metil yang paling jauh dari gugus fungsional, karena menunjukkan perisai yang lebih baik, pergeseran kimia yang lebih rendah, dan multiplisitas yang sesuai.
Kromatografi cair kinerja tinggi
Sistem reaksi dianalisis dengan kromatografi untuk mengonfirmasi pembentukan ester secara kualitatif, khususnya etil oleat sebagai produk utama. Puncak dalam kromatogram (Gbr. 8 ) sesuai dengan etil oleat yang terbentuk melalui reaksi enzimatik. Dalam kromatografi fase terbalik, senyawa yang kurang polar berinteraksi lebih kuat dengan fase stasioner, sedangkan fase gerak polar mengeluarkan komponen yang lebih polar. Absorbansi maksimum untuk setiap komponen ester diamati pada 254 nm.
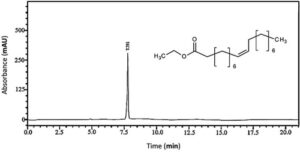
Etil oleat memiliki rantai karbon yang panjang, yang membuat molekul ini memiliki polaritas yang rendah. Semakin panjang rantai karbon suatu ester, semakin besar interaksinya dengan kolom nonpolar. Puncak tersebut dikaitkan dengan produk esterifikasi yang signifikan dalam media reaksi, yang memiliki polaritas terendah dan interaksi yang kuat dengan kolom fase terbalik. Oleh karena itu, faktor retensi tertinggi dikaitkan dengan senyawa ini. Sebaliknya, ester lain dengan rantai yang lebih pendek dan konsentrasi rendah akan memiliki faktor retensi yang lebih rendah, yang menunjukkan afinitas yang lebih besar terhadap pelarut polar.
Kesimpulan
Studi ini secara efektif menjelaskan interaksi antara lipase Eversa Transform 2.0 dan substrat potensial yang relevan dengan produksi biodiesel, termasuk sumber yang terbarukan dan ramah lingkungan seperti komposisi lipid minyak ikan. Melalui analisis in silico , kami menunjukkan bahwa asam miristat dan asam oleat berikatan secara proksimal dengan situs aktif enzim, menunjukkan energi bebas yang menguntungkan, dan membentuk ikatan hidrogen, alkil, dan interaksi π -alkil yang spesifik.
Simulasi dinamika molekular menggarisbawahi stabilitas yang kuat dan nilai RMSD minimal, yang mengonfirmasi kesesuaian postur pengikatan yang dipilih untuk terjadinya reaksi tanpa hambatan. Meskipun demikian, sementara simulasi komputasional berfungsi sebagai alat penyaringan awal yang berharga, penerapan secara in vitro dan aplikasi yang lebih luas menghadapi variabel dan tantangan tambahan.
Tantangan-tantangan ini mencakup berbagai faktor seperti kondisi transportasi, aktivitas katalitik, penghambatan enzimatik, kondisi keseimbangan, dan sifat fisikokimia biodiesel yang dihasilkan. Mengatasi kompleksitas ini memerlukan studi komprehensif lebih lanjut dan pertimbangan cermat untuk memastikan penerapan proses produksi biodiesel yang dimediasi lipase secara efektif dan berkelanjutan.




Tinggalkan Balasan